突破内卷围城,国产创新药闯关2万亿市场!
- 2022-04-30 10:30:10 医药网
- 独家
4月30日,FDA将公布和黄医药的索凡替尼以及君实生物的特瑞普利单抗2款国产新药在美上市审评结果。纵观历史,我国创新药出海可以中国加入ICH为维度来划分,目前BIC和FIC类创新药遇上赛道黄金时机。自2017年中国加入ICH以来,在美提交上市申请的国产创新药已超过10款,超10亿元的License-out项目也达到10个,未来创新药出海更显常态化。
出海探索:上市热潮迭起
1959年3月,复星医药的双醋酸曲安西龙在美国获批(NDA),成为我国创新药出海的最早尝试。2019年11月,我国创新药出海再次迎来喜讯,百济神州的泽布替尼获美国FDA批准上市,成为首个成功出海的国产抗癌创新药。该药获批后很快获得了国际市场的认可,企业年报显示,2021年泽布替尼的全球销售额达2.18亿美元(以4月25日汇率计,约14亿元),同比增长423%。
在百济神州的泽布替尼之前,国内绝少有本土创新药能成功出海。业内专家表示,除了“7·22”所揭露的真实性问题以外,以往中国很多临床数据都是在非ICH(国际人用
ICH能实现包括数据在内的标准指南逐步互认,免去了很多进出口的再注册程序,加速药品创新和上市。据不完全统计,目前已有数十款国产创新药在美国提交NDA/BLA,其中泽布替尼、马来酸左旋氨氯地平以及西达基奥仑赛3款药品已经获批上市。
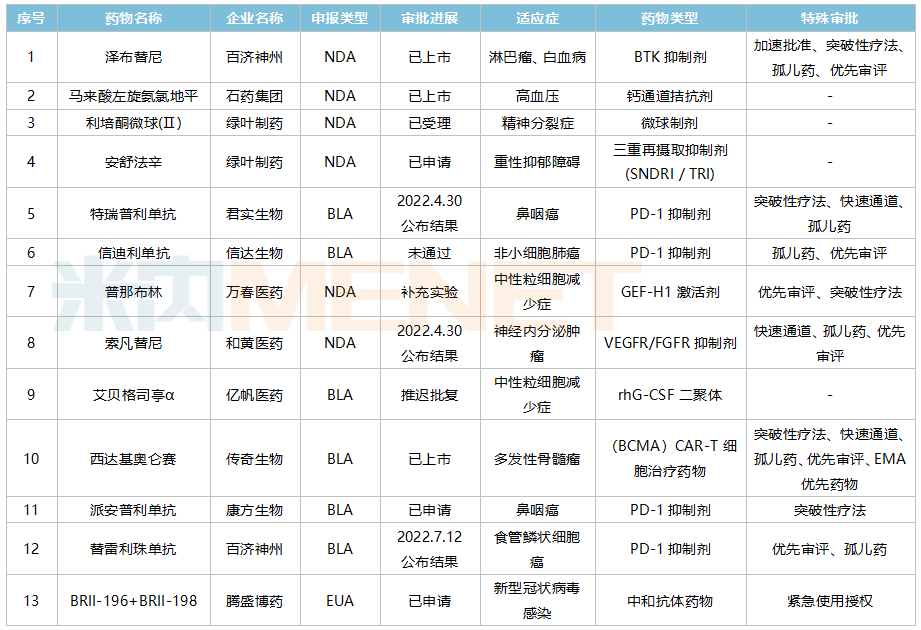
国产创新药FDA上市申请情况(部分)

来源:米内网整理
马来酸左旋氨氯地平为石药集团的改良型创新药,2019年在美上市。与辉瑞的氨氯地平相比,左旋氨氯地平安全性上更胜一筹。2022年初,传奇生物的西达基奥仑赛再次铸造了国产新药出海里程碑式突破,该药直接对标蓝鸟的Abecma,从临床数据来看,西达基奥仑赛在针对R/R MM患者在缓解率与完全缓解率方面更优。
国产创新药出海也有受阻的时候,在西达基奥仑赛上市之前,信达生物的信迪利单抗因药物临床价值以及临床试验单一性被FDA拒之门外,但在印尼的商业化布局以及驯鹿医疗合作开发的等出海项目上,信达生物依然稳步推进。
万春医药的普那布林也被卡在单一临床试验结果,根据披露的数据,普那布林87%的患者临床数据来源于中国,因此FDA要求其进行第二项试验。目前普那布林在国内的上市申请已纳入优先审评,该药可能会率先在国内上市。不过万春医药曾公开表示对普那布林的安全性以及疗效充满信心,并计划开展第二项试验,未来有望实现在美上市。
此外,疫情环境也给本土创新药出海造成一定的阻碍,亿帆医药曾表示,FDA受疫情影响无法来到国内对企业的艾贝格司亭α进行生产现场检查,因此造成该药的推迟批复。按时间来划分,FDA将在2022年4月末与7月分别公布索凡替尼、特瑞普利单抗、替雷利珠单抗等药物的上市审评结果。
值得注意的是,在全球范围内,PD-1/L1等创新药存在过度开发的问题,目前FDA已逐步收紧对此类创新药的上市门槛。业内统计,2021年10个进入FDA加速审批通道的PD-1单抗适应症中,有7个主动或被撤回。未来,FDA有可能将会加强对PD-1/L1等候选药物“头对头”研究等临床试验的审评审批。
License-out:加速技术通关全球
对于目前国内大多数创新药企业来说,能够完整拥有自主海外销售团队的企业仍在少数,License-out模式能够让本土创新药企更快融入国际市场,并将技术成果变现转化。2007年3月,微芯生物将其在研产品西达本胺在中国以外的全球开发权益以2800万美元的价格授权给了美国HUYA公司,开创了中国创新药License-out的先河。后在2015年9月,恒瑞医药以7.95亿美元的交易总额,将其PD-1抗体药物卡瑞利珠单抗的国外权益出售给美国因塞特公司(INCYTE),这是中国企业首次对外转让创新生物药品。
随着药械审评审批改革制度的发布以及海外人才的不断引进,创新药进出口环境得到进一步开放,License-out数量急剧增长,在2017年中国加入ICH后,创新药License-out更显常态化。据不完全统计,目前国内医药行业已有超过50个License-out交易,其中2018年国内创新药企发生9起,数量创了新高,授权方主要为恒瑞、豪森、复星、科伦等传统头部企业。此后,百济神州、天境、信达以及基石等一批“新贵”在国际市场“崭露锋芒”。从2021年开始,高诚、锐格、索元以及普瑞金等更多新面孔也开始涌现,当年全年License-out交易超过30个,共披露的交易金额约为133亿美元。
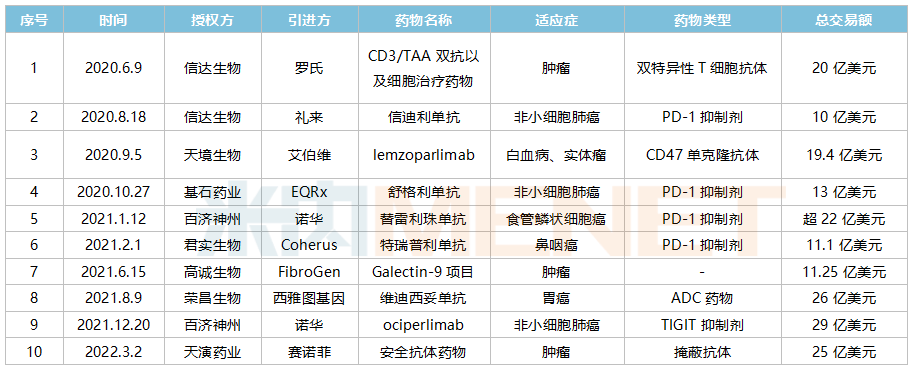
近年国产创新药超10亿美元License-out项目(部分)

来源:米内网整理
2021年初,百济神州宣布与诺华就替雷利珠单抗在多个国家的开发、生产与商业化达成合作与授权协议,百济神州获得了高达6.5亿美元的首付款,一举刷新了国内License-out交易的首付款纪录。2021年末,百济神州再次宣布与诺华达成重磅交易,百济神州将TIGIT抗体的主要海外权益以29亿美元的价格授权给了诺华,再次刷新中国药企单品种对外授权金额新高。
除了百济神州,荣昌生物、天演生物等企业也表现亮眼。2021年8月,荣昌生物以26亿美元的价格将维迪西妥单抗授权给西雅图基因,成为国产ADC药物License-out第一例。最近,赛诺菲以25亿美元的潜值金额与天演生物合作,根据天演生物的抗体精准掩蔽SAFEbody技术合作开发掩蔽抗体药物,在此之前Exelixis、田边研究所等众多国际机构也向天演生物寻求合作......
从海外发展经验来看,License-out模式主要聚焦于新兴的Biotech企业,授权企业可从授权药物获得里程牌付款和销售分成等费用,快速实现“自我造血”,并且这种合作模式也能为授权企业降低研发成本。但也有不少人认为,长期以License-out为主的商业化模式难以支持企业保持长久稳定的盈利收入,与此同时还要求企业必须具备丰富且尖端的技术储备,因此这种模式对于企业市值增长以及可持续化运营方面具有较大的难度。
踏浪前行:登岸无捷径可图
从长期角度来看,国内沿着美国Biotech为主的发展并不太现实,在起点上国内药企就以仿制和改良为主,并且目前国内新晋的创新药企不会满足于产品和技术授权,不少企业的意愿一开始就朝着全职的Biopharma目标发展,这也意味着国内创新药企必须要将市场面向全球。业内曾统计,尽管目前中国患者基数大,但医药市场占全球比重不足20%,并且针对创新药市场而言,在支付体系等因素影响下,目前以美国为首的全球市场占比超过80%,市场规模已超过2万亿元,而中国在内的新兴国家却不及2%。此外,国内已出现了较为严重的“内卷”情况,并且医保杀价下让持续收窄利润空间进一步压缩,直接推动国内众多创新药企奔赴欧美等国际市场,以谋求更大的升值与发展空间。
其次我国加入ICH之后,国内创新药审评审批指导原则也紧跟国际标准来衡量,按照ICH的E17(多区域临床试验原则)标准执行,国内创新药也将会被反推走向国际市场。纵观全球新药领域,美国FDA的法规要求是全球范围内具有代表性的成熟药品监管“标准”,并且相对于同样成熟的欧盟,美国FDA对创新药的开放程度以及审批效率更高,在美国FDA“镀金”过的新药能较快实现在全球大多数市场流通,因此美国成为我国乃至全球创新药出海上市的首要选择地区。百济神州全球总裁吴晓滨曾向媒体表示:“走向发达国家地区是对能力的证明,但发展中国家更加缺医少药,这恰恰是创新药企能够给这些国家和人民带来巨大利益的着力点。”
对于创新药企来说,国际化没有捷径可走。若要一款创新药成功“出海登岸”,过硬的技术、强大的团队、雄厚的资本仅是创新药企必备的硬性条件。在此基础上,企业更需在临床需求、药物疗法等方面具有前瞻性视野,根据自身优挖掘核心竞争力与独特优势,围绕临床价值为中心实现差异化布局。并且,企业从研发立项、临床设计再到临床试验每一步过程都需严格按照国际标准执行,在此期间与FDA保持充分的沟通,最大程度降低风险,这也是目前国际大药企都在FDA办公所在地的马里兰附近设办公室的原因。
结语
总的来看,“后ICH”时代下,我国创新药出海更显活力,像百济神州、君实等首批出海探索的企业在2021年海外商业化方面均展现出亮眼的成绩。从宏观导向来看,未来国产创新药国际化将成为定势,由此进一步引导创新药企回归临床需求本质,寻求新靶点新疗法的突破。目前,国内创新药出海主要聚焦在小分子与生物药两大领域,但在国产特色的中成药方面却难以突破,迄今为止,尚无国产中成药在美国上市。部分专家认为,中成药出海需从品控以及临床两大方面着力,并且市场也应给中成药更多耐心,未来如何仍需要时间去验证。
数据来源:公司公告、米内网整理
注:数据统计截至4月25日,如有疏漏,欢迎指正!

本文地址:http://www.bx9y.com/dujia/2022-04-30/587552.html
友情提示:文章内容为作者个人观点,不代表本站立场且不构成任何建议,本站拥有对此声明的最终解释权。如果读者发现稿件侵权、失实、错误等问题,可联系我们处理
健康快报
7*24小时快讯
- 黑龙江新增本土确诊病例10例 新增本土无症状感染者237例2022-11-17 18:00:32
- 河北新增无症状感染者263例2022-11-17 18:00:32
- 山东新增本土确诊病例16例、本土无症状感染者151例2022-11-17 18:00:31
- 31省份新增本土确诊病例2328例、本土无症状感染者20804例2022-11-17 18:00:31
- 明年迎来1158万毕业生 教育部多举措促就业2022-11-17 18:00:31
健康图文排名
-

 灵活就业人员社保缴费怎么交?2022年灵活就业人员社保缴费多少钱?
灵活就业人员社保缴费怎么交?2022年灵活就业人员社保缴费多少钱?
2022-06-13
-

 五险一金多少钱?五险一金缴费标准是多少?
五险一金多少钱?五险一金缴费标准是多少?
2022-07-01
-
2022年社保缴费基数六个档次是什么?每个月扣多少钱
2022-06-30 15:21:11
-
7类人不用隔离14天 原来这些人不用集中隔离
2022-05-06 11:19:41
-
2022年五险一金缴费标准最低是多少?五险一金一个月大概交多少钱?
2022-08-11 09:40:26
-
境外人员回国隔离新规2022:具体需要隔离几天?回国隔离新规放松!
2022-07-01 15:01:46
-
2022中国首富是谁排名第一 来揭晓答案
2022-05-09 15:20:17


