胰岛素龙头猛攻创新药,20亿大品种抢国产首家!
- 2023-03-11 10:30:18 医药网
- 独家
近期,国产胰岛素龙头通化东宝再传捷报,URAT1抑制剂(THDBH130片)Ⅱ期临床试验完成首例受试者入组。近年来,通化东宝持续加码研发,猛攻创新药,实现对胰岛素类似物注射液、GLP-1受体激动剂、高临床价值口服降糖药品研发的全覆盖。2022年拿下3款重磅新品;2款产品报产在审,20亿大品种利拉鲁肽注射液抢国产首家。此外,公司多渠道布局,国产胰岛素扬帆出海,GLP-1/GIP双受体激动剂(注射用THDBH121)申报临床、人胰岛素注射液在欧盟申报上市均获受理。
猛攻创新药,胰岛素、GLP-1、口服降糖药全覆盖

来源:米内网新版数据库
近日,通化东宝发布公告,其全资子公司东宝紫星(杭州)生物医药的化药1类新药URAT1抑制剂(THDBH130片)已经顺利完成I期临床试验,已启动中国II期临床试验,并于近日成功完成首例受试者入组。THDBH130片是一种特异性作用于尿酸排泄通路的高活性、高选择性、高安全性的尿酸转运体URAT1抑制剂,I期临床试验结果显示其具有低系统暴露、高药理学活性、餐后给药更优的降尿酸效应特点,具有良好的安全性及耐受性。
目前,以URAT1为靶点的排尿酸药物主要有苯溴马隆和雷西那德。米内网数据显示,2021年三大终端6大市场(统计范围见文末)抗痛风制剂合计销售规模超过20亿元,苯溴马隆是TOP2品种,雷西那德未在国内上市。
据了解,此次启动“一项在成人高尿酸血症伴或不伴痛风患者中评价THDBH130片的安全性、耐受性,初步临床有效性及药代/药效动力学特征的多中心、随机、双盲、安慰剂和苯溴马隆对照IIa期临床研究”,主要目的是评估口服THDBH130片安全性、耐受性和初步有效性;次要目的包括评估降尿酸作用、对患者痛风发作的影响及药代/药效动力学特征。截至公告日,公司在该项目中研发投入约4023.52万元。
通化东宝部分在研项目情况
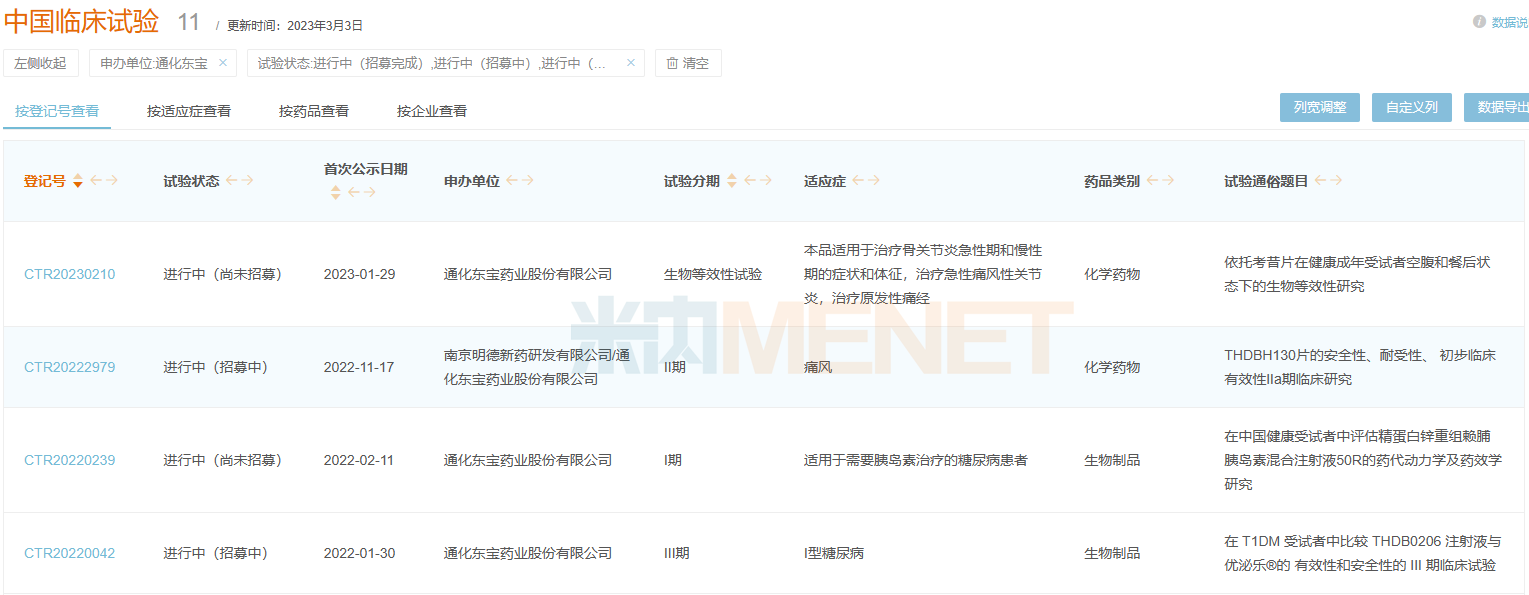

来源:米内网新版数据库
通化东宝深耕糖尿病治疗领域,在不断巩固国产胰岛素龙头地位的同时,优化在研产品结构,实现对胰岛素类似物注射液、GLP-1受体激动剂、高临床价值口服降糖药品研发的全覆盖。公司2022年前三季度研发费用1.12亿元,占营收比例超过5%,研发费用已超过2020年全年。
通化东宝聚焦创新研发,布局前沿靶点及疗法,扩大产品适应症、拓展治疗领域,在研项目中有3款糖尿病治疗领域1类新药、2款痛风/高尿酸血症治疗领域1类新药以及痛风治疗领域化学口服药物。在研产品中的THDBH120/121、THDBH110/111、索马鲁肽注射液等品种涵盖降糖、减肥等多个适应症。
值得注意的是,通化东宝近年积极拓展布局痛风/高尿酸血症领域,将结合公司现有的糖尿病慢病管理平台,未来将形成良好的协同效应。去年9月,公司的化药1类新药THDBH151片获批临床,该产品是痛风双靶点抑制剂,此前国内外均暂无同类产品上市。
3大重磅新品冲击超600亿市场,20亿大品种抢国产首家
2022年通化东宝获批产品情况
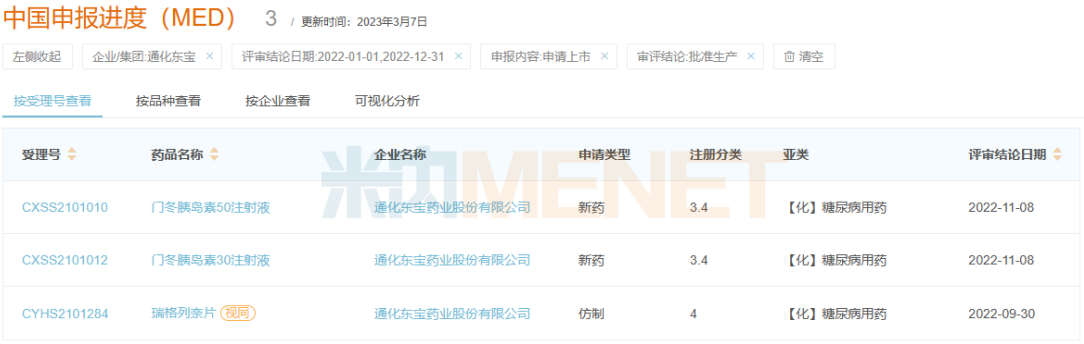
来源:米内网新版数据库
2022年,通化东宝有门冬胰岛素50注射液、门冬胰岛素30注射液、瑞格列奈片3款新品获批,进一步丰富公司在糖尿病用药领域的产品管线。米内网数据显示,2021年三大终端6大市场糖尿病用药市场规模超过600亿元。
瑞格列奈片是通化东宝第3款获批的口服降糖药,在此之前,公司已拿下磷酸西格列汀片和西格列汀二甲双胍片(Ⅱ),均在2021年获批。门冬胰岛素50注射液和门冬胰岛素30注射液获批则实现公司在门冬胰岛素系列产品的布局,其中,门冬胰岛素50注射液是国产首家,2021年三大终端6大市场门冬胰岛素合计销售规模超过90亿元。
通化东宝产品报产在审情况
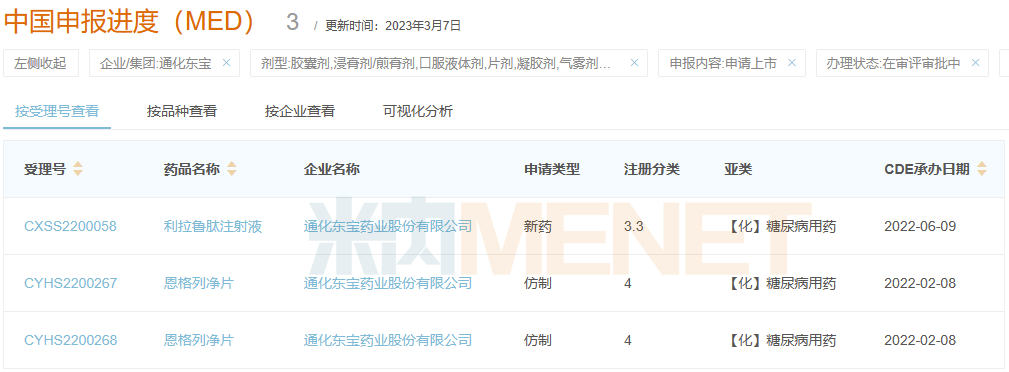
来源:米内网新版数据库
目前,通化东宝的有2款报产在审。2021年三大终端6大市场利拉鲁肽注射液销售规模近20亿元;恩格列净片则潜力惊人,2020年-2021年销售额分别同比增长324.45%、179.51%。
近年三大终端6大市场利拉鲁肽注射液销售情况(单位:万元)
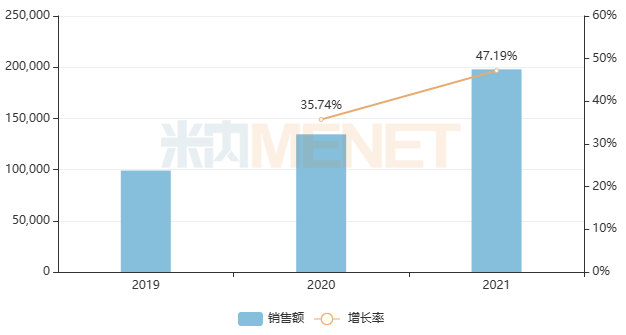
来源:米内网格局数据库
利拉鲁肽是一种人胰高血糖素样肽-1(GLP-1)类似物,可激活人GLP-1受体,促进胰腺分泌胰岛素。该品种由诺和诺德研发,2011年进入中国市场。2021年三大终端6大市场销售额近20亿元,同比增长超过40%。目前,国内仅有诺和诺德拥有生产批文,通化东宝、杭州中美华东制药、江苏正大天晴药业等6家报产在审。
资料显示,2018年9月,通化东宝获得国家药监局核准签发的利拉鲁肽原料药审批意见通知件、利拉鲁肽注射液药物临床试验批件;2020年7月,获得Ⅰ期临床试验总结报告;2021年10月,获得Ⅲ期临床试验总结报告;2022年6月,利拉鲁肽注射液报产获受理,公司在该项目已投入研发费用超过2亿元。
2022年12月,通化东宝与科兴制药签署《利拉鲁肽海外市场独家许可合作协议》,科兴制药获得利拉鲁肽在新兴市场共17个国家的独家商业化许可权益。日前,科兴制药接受机构调研时表示,该产品预期在2023年Q4在国内获批,公司正在推进利拉鲁肽在海外市场的客户筛选工作,产品获批上市后将迅速启动海外注册。
多渠道布局,国产胰岛素扬帆出海

今年以来,通化东宝捷报频传,多渠道布局,国产胰岛素扬帆出海。GLP-1/GIP双受体激动剂(注射用THDBH121)申报临床、人胰岛素注射液在欧盟申报上市均获受理。
1月,化药1类新药GLP-1/GIP双受体激动剂(注射用THDBH121)申报临床获受理,该产品是胰高血糖素样肽-1(GLP-1)受体和葡萄糖促胰岛素分泌多肽(GIP)受体双靶点激动剂,其将GLP-1和GIP这两种促胰岛素的作用整合至一个多肽单分子中,且通过分子设计进一步提高代谢稳定性,发挥协同促进的血糖控制、体重减轻以及调节脂质代谢等功能,满足单一分子靶点或复方制剂治疗效果不佳的糖尿病患者的临床需求,有望成为更长效的治疗糖尿病和肥胖的重磅药物。
2月,人胰岛素注射液在欧盟申报上市获受理,通化东宝负责提供胰岛素原料药,瑞康公司使用通化东宝提供的胰岛素原料药生产人胰岛素注射液。通化东宝表示,公司近年稳步推进人胰岛素及胰岛素类似物的海外注册工作,该产品如顺利获批,将成为公司胰岛素产品积极开拓发达国家市场的里程碑事件,同时加速公司人胰岛素产品在海外多个国家的注册进程,促进公司人胰岛素产品的海外销售,进一步开拓国际市场空间。
资料来源:公司公告、米内网数据库
分享:

本文地址:http://www.bx9y.com/dujia/2023-03-11/658018.html
友情提示:文章内容为作者个人观点,不代表本站立场且不构成任何建议,本站拥有对此声明的最终解释权。如果读者发现稿件侵权、失实、错误等问题,可联系我们处理




